Алкины | Конспект
Конспект
Алкины – это непредельные УВ с общей формулой \(C_{n}H_{2n - 2}\), содержащие \(\equiv\) связь.
Пропин
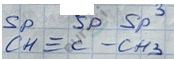
Этин, ацетилен
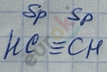
Особенности строения
1) Sp – гибридизация атомов С при \(\equiv\) связи.
2) Форма молекул линейная

3)

4) Валентный угол \(\sim\) 180°
5) \(l_{C \equiv C}\) \(\sim\) 0,120 Нм
Изомерия алкинов
Структурная:
1) С-скелета

2) Положения \(\equiv\) св.
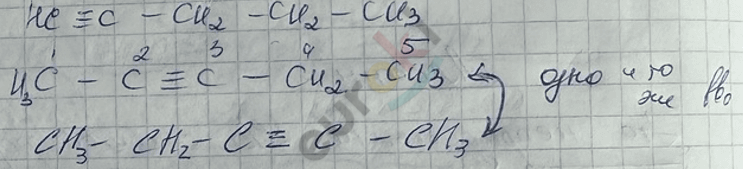
3) Межклассовая
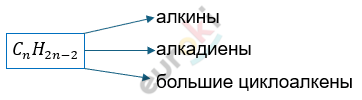
Химические свойства алкинов
I. Реакция присоединения
1) реакция гидрирования
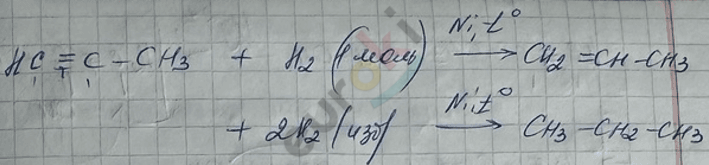
2) реакции с \(\text{Br}_{2}\) (\(H_{2}O\)), \(I_{2}\) (\(H_{2}O\)), \(\text{Cl}_{2}\) (без условий, без катализаторов).
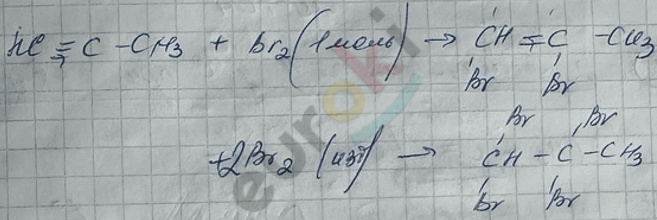
3) реакция гидрогалогенирования (без катализаторов).
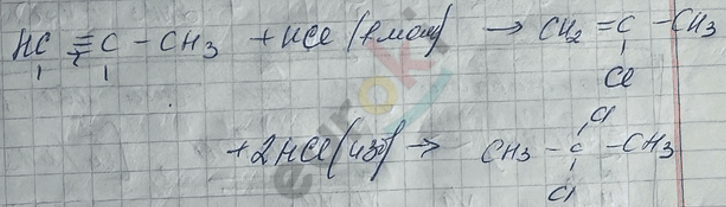
4) реакция гидратации (реакция Кучерова)
Только ацетилен с \(H_{2}O\) даёт ацетальдегид, а все остальные алкины дают кетоны.


II. Реакция замещения атомов Н у С при \(\equiv\) связи.
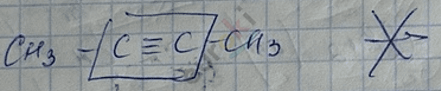
а)
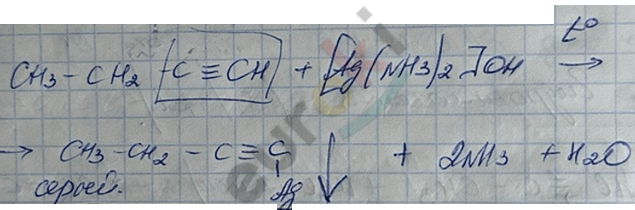
Реактивами для этой реакции являются:

б)

III. Реакция полимеризации
1) димеризация ацетилена

2) тримеризация алкинов
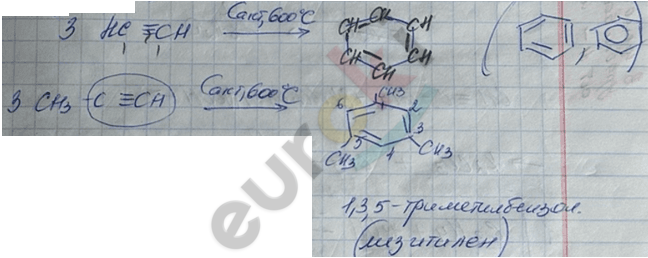
IV. Реакция окисления
1) реакция горения
2) под действием химических окислителей \(\text{KMnO}_{4}\), \(K_{2}\text{Cr}_{2}O_{7}\), \(K_{2}\text{CrO}_{4}\)
а) очень мягкое окисление \(С_{2}Н_{2}\) под действием \(\text{KMnO}_{4}\), \(Н_{2}О\) при охлаждении.
Только для ацетилена

В щелочной среде недостаток атомов О уравнивают -ОН группами (удвоением), недостаток атомов Н – молекулами \(Н_{2}О\).
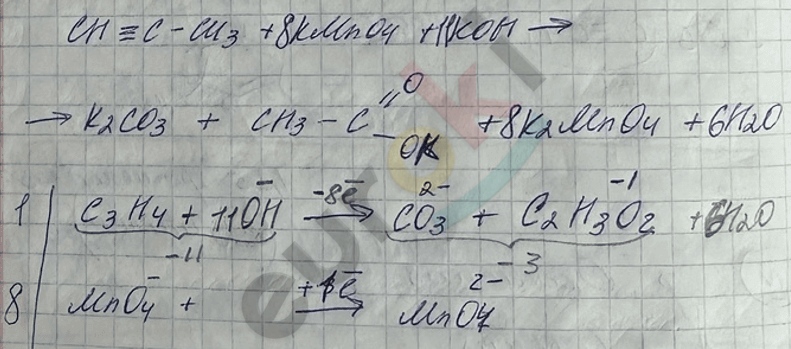
Получение алкинов
1*) Карбидный метод получения \(С_{2}Н_{2}\)

2*) 2 \({СН}_{4}\) \(СН\) \(\equiv\) \(СН\) + \({3Н}_{2}\)
3)
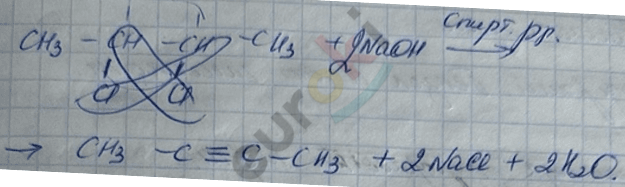
4) реакция увеличения длины цепи у алкина
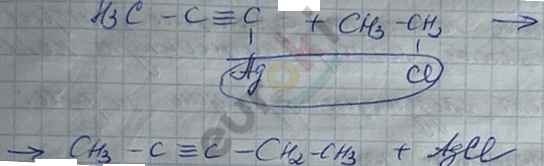
5)

Нефть – маслянистая жидкость тёмно-коричневого или чёрного цвета, представляет собой смесь жидких УВ.
Не смешивается с водой.
Отделить нефть от воды можно с помощью делительной воронки.
По составу нефть бывает 3 видов:
1) парафиновая – состоит из алканов с прямой и разветвлённой цепью;
2) нафтеновая;
3) ароматическая.


