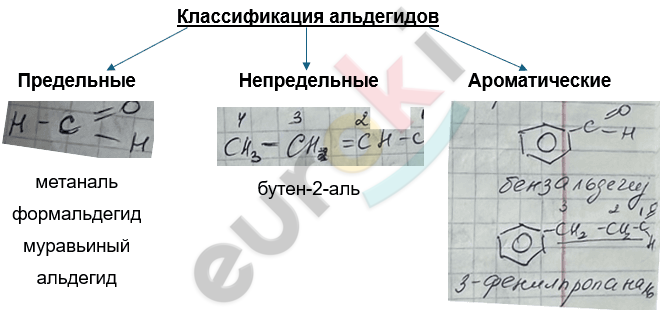
Альдегиды | Конспект
Конспект

Альдегиды водородных связей не образуют => 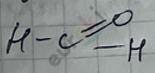 – это газ ↑, с характерным запахом, хорошо растворим в воде, его 30–40% раствор называют формалином.
– это газ ↑, с характерным запахом, хорошо растворим в воде, его 30–40% раствор называют формалином.
Остальные альдегиды – жидкие вещества.
Изомерия предельных карбонильных соединений
1) С-скелета

2) Межклассовая изомерия

3) У кетонов
а) изомерия положения кетогрупп

б) изомерия радикалов

Химические свойства
I. Реакция присоединения
1) реакция гидрирования (реакция восстановления)
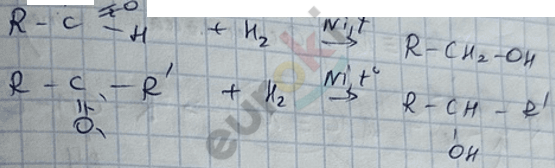
2) реакция с \(\text{NaHSO}_{3}\)
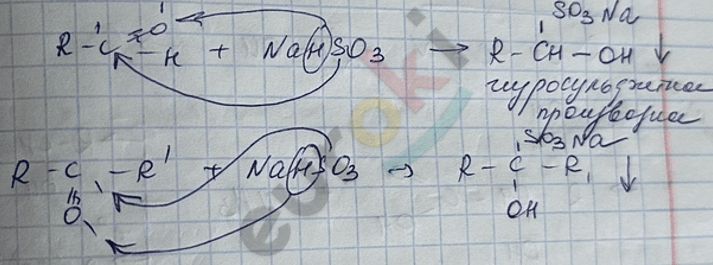
3) реакция со спиртами с получением полуацеталей и ацеталей
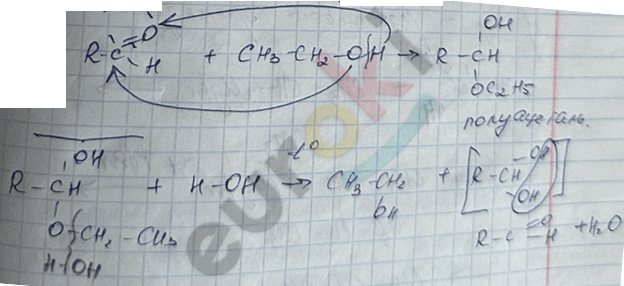
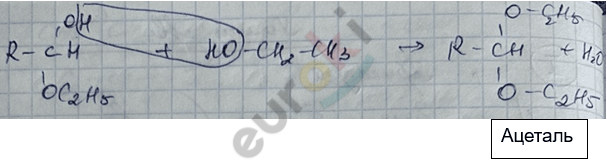
4) реакция с HC \(\equiv\) N (синильная кислота)
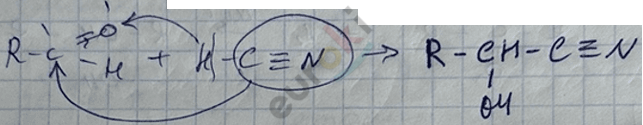
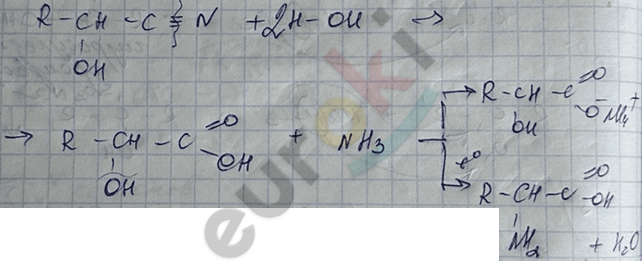
5) реакция с реактивом Гриньяра
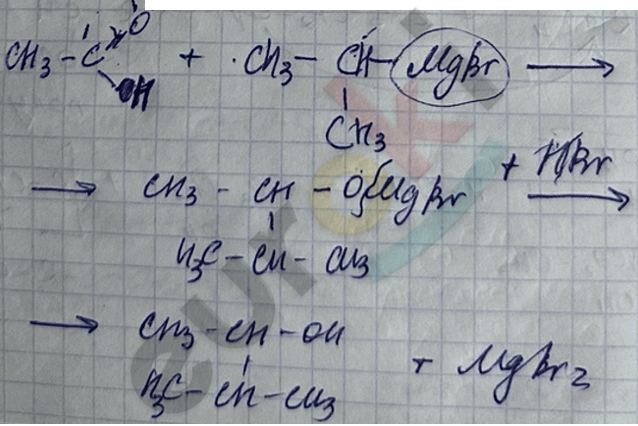
II. Реакция окисления
1) реакция горения

2) каталитическое окисление \(O_{2}\) (катализатор), только альдегиды
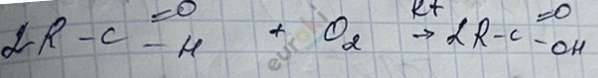
3) только для альдегидов
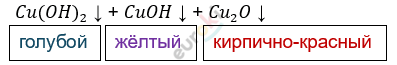
а) реакция «серебряного зеркала»

б) реакция «медного зеркала»

В этой реакции идёт последовательное превращение
в) реакция с \(\text{Br}_{2}\)(\(H_{2}O\))
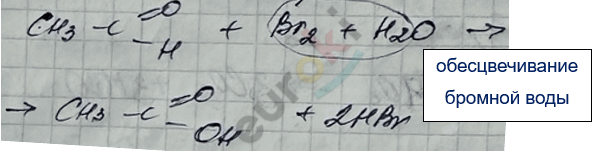
г) реакция с \(\text{KMnO}_{4}\) (\(H^{+}\), \(H_{2}O\), \(\text{OH}^{-}\)), \(K_{2}\text{Cr}_{2}O_{7}\) (\(H^{+}\)), \(K_{2}\text{CrO}_{4}\) (\(H_{2}O\), \(\text{OH}^{-}\))
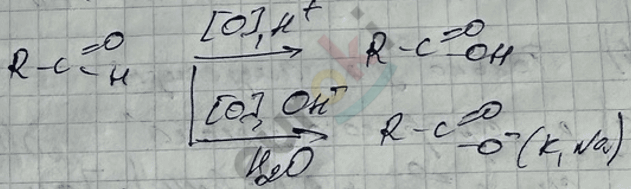
III. Реакция полимеризации для 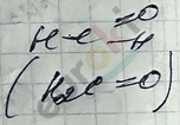
а) линейная

б) циклическая
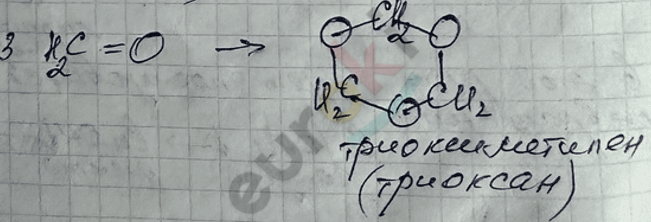
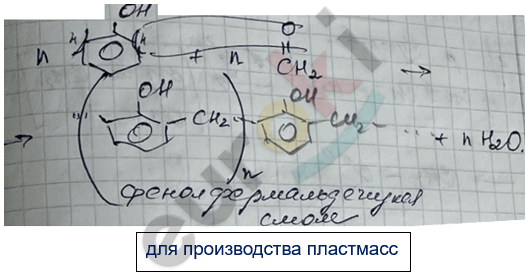
IV. Реакция поликонденсации
V. Реакция с \(\mathbf{\text{PCl}}_{\mathbf{5}}\)



